Moderna pide aplicar ya su vacuna para salvar vidas: su eficacia sube al 100 % en casos de Covid graves
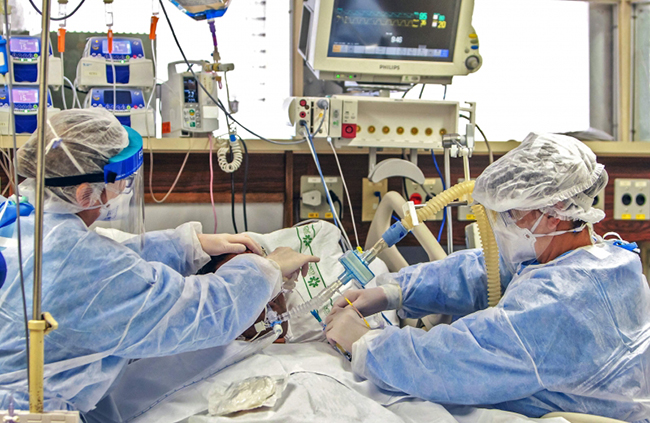
Los hospitales estadounidenses han llegado a su límite mientras la nación registra más de 160.000 casos nuevos al día y más de 1.400 decesos diarios. Desde que surgió por primera vez hace un año en China, el virus ha provocado la muerte de más de 1,4 millones de personas en el mundo. Se espera que la vacuna pueda poner punto final a esta pandemia.
New York. Associated Press. Moderna Inc. pidió a los reguladores de Estados Unidos y de la Unión Europea que permitan el uso de emergencia de su vacuna contra COVID-19, luego de que nuevos resultados confirmaron que ofrece una protección sólida, intensificando la carrera para empezar a administrar las inyecciones mientras la pandemia de coronavirus avanza. Varias candidatas a vacuna deben tener éxito para que el mundo ponga alto a la pandemia, que ha tomado un segundo aire en Estados Unidos y Europa.
Moderna está detrás de Pfizer y su socia alemana BioNTech en los intentos para empezar a vacunar a la población estadounidense en diciembre. Los reguladores británicos también están evaluando la inyección de Pfizer y otra de la asociación entre Universidad de Oxford y AstraZeneca.
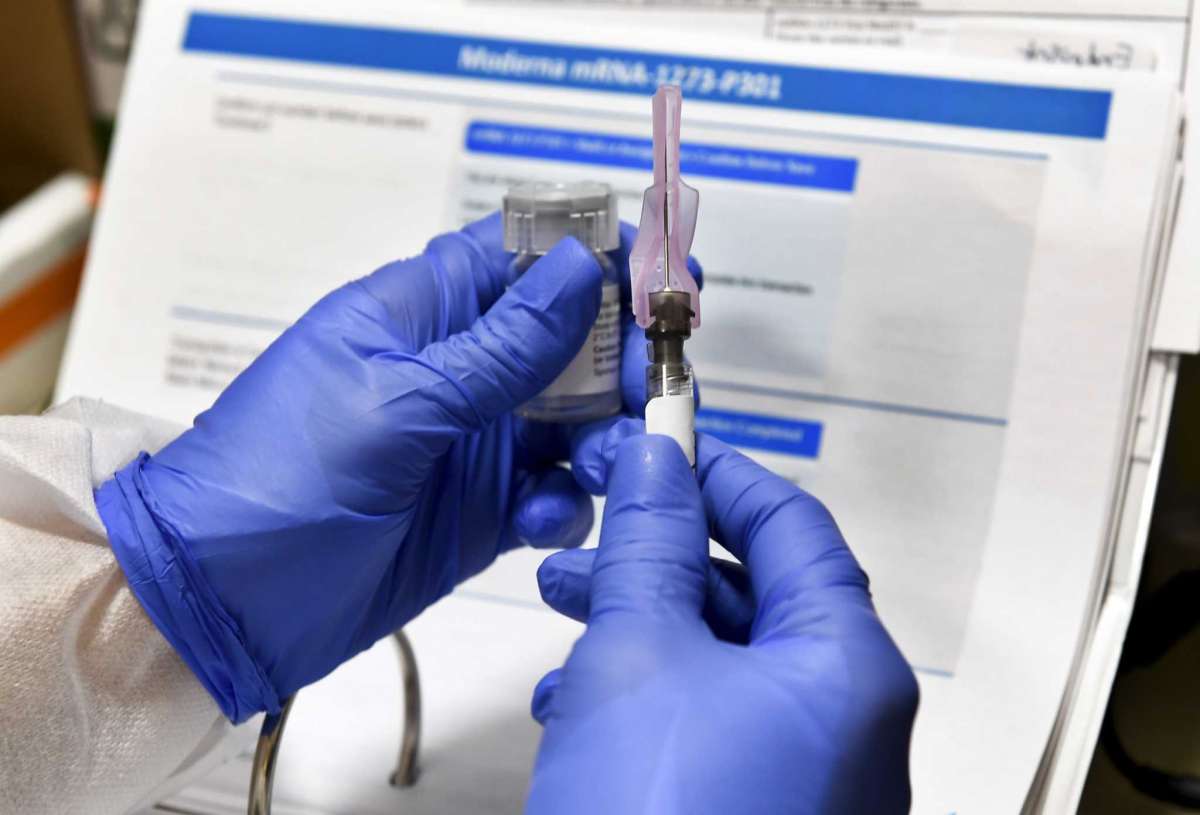
Moderna creó sus dosis con los Institutos Nacionales de la Salud de Estados Unidos y ya había obtenido buenas señales mientras estaba trabajando, pero dijo que obtuvo los resultados finales que necesitaba durante el fin de semana, que muestran que la vacuna tiene una efectividad de más del 94%.
De los 196 casos de COVID-19 involucrados en este enorme estudio, 185 fueron participantes que recibieron placebo y 11 que les administraron la vacuna real. Los únicos que se enfermaron de gravedad —30 participantes, entre ellos uno que falleció— habían recibido vacunas falsas, dijo el médico Tal Zaks, el director médico de la compañía con sede en Cambridge, Massachusetts.
Cuando supo de los resultados, “me permití llorar por primera vez”, comentó Zaks a The Associated Press. “Tan sólo en el ensayo, ya hemos salvado vidas. Imaginen el impacto cuando se multiplique a la gente que pueda obtener esta vacuna”.
Moderna dijo que la efectividad de la vacuna y un buen historial de seguridad, con efectos secundarios temporales parecidos a los síntomas de la influenza, significan que la farmacéutica ha cumplido con los estándares fijados por la Administración de Alimentos y Medicamentos de Estados Unidos (FDA por sus siglas en inglés) para un uso de emergencia antes de que se finalice la etapa final de pruebas. La Agencia Europea de Medicamentos ha señalado que también está dispuesta a dar una autorización “condicional”.
La FDA ha prometido que antes de que decida desplegar cualquier vacuna contra el COVID-19, sus asesores científicos debatirán públicamente si hay suficiente evidencia detrás de cada candidata a vacuna.
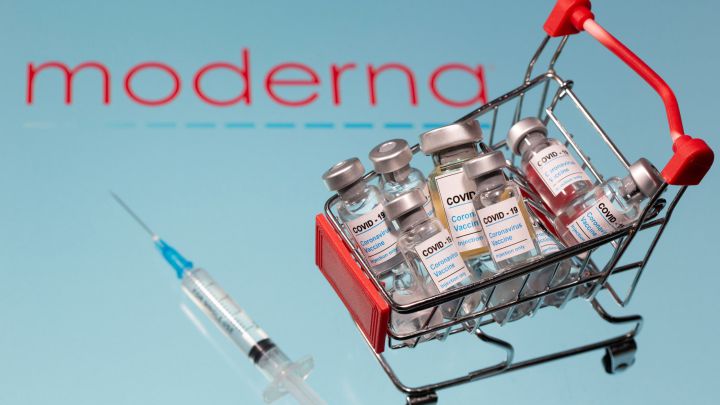
El Departamento de Salud y Ciencia de The Associated Press recibe el apoyo del Departamento de Educación Científica del Instituto Médico Howard Hughes. La AP es la única responsable de todo el contenido.
Moderna anunció los resultados de la fase 3 de su vacuna mRNA-1273, en cuyos ensayos han participado 30.000 participantes. De ellos, 196 se infectaron de Covid, 30 de ellos de forma severa.
De los 30 casos que presentaron un cuadro grave de Covid, todos había recibido placebo, por lo que la compañía ha anunciado un 100% de eficacia de protección frente a los casos más graves de SARS-CoV-.
De los 196 casos infectados, 185 se habían incluido en el grupo que recibió placebo y 11 en el que recibió la vacuna de Moderna, basada en RNA mensaje, por lo que la farmacéutica concluye que la eficacia de inyección es del 94,1%.
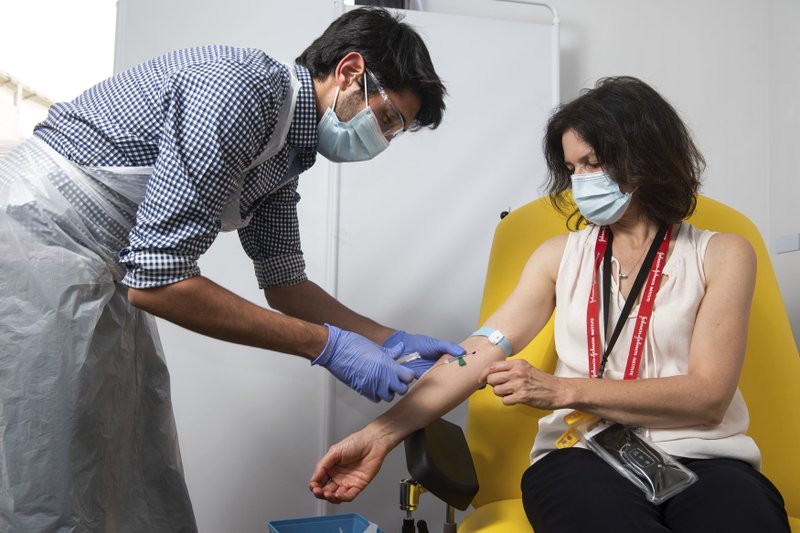
Moderna solicitó Autorización de Uso de Emergencia a la FDA, y, posteriormente, se prevé que el 17 de diciembre, Moderna se reúna con el Comité Asesor sobre Vacunas y Productos Biológicos (VRBPAC por sus siglas en inglés) para analizar la seguridad y eficacia de la vacuna candidata.
Al mismo tiempo, solicitará una aprobación condicional de la vacuna a la EMA. Y, para apoyar estas peticiones, la compañía ha informado de que tiene la intención de obtener por parte de la Organización Mundial de la Salud (OMS) la pre calificación (PQ) de su vacuna y que se incluya en su Listado de Uso de Emergencia.
Con los datos obtenidos, Moderna señala que los resultados son consistentes tanto por grupos de edad, etnia o género. «Este positivo análisis primario confirma la capacidad de nuestra vacuna para prevenir la enfermedad COVID-19 con una eficacia del 94,1% y, lo que es más importante, la capacidad de prevenir la grave enfermedad COVID-19. Creemos que nuestra vacuna proporcionará una nueva y poderosa herramienta que puede cambiar el curso de esta pandemia y ayudar a prevenir enfermedades graves, hospitalizaciones y muertes», ha señalado Stéphane Bancel, director ejecutivo de Moderna.
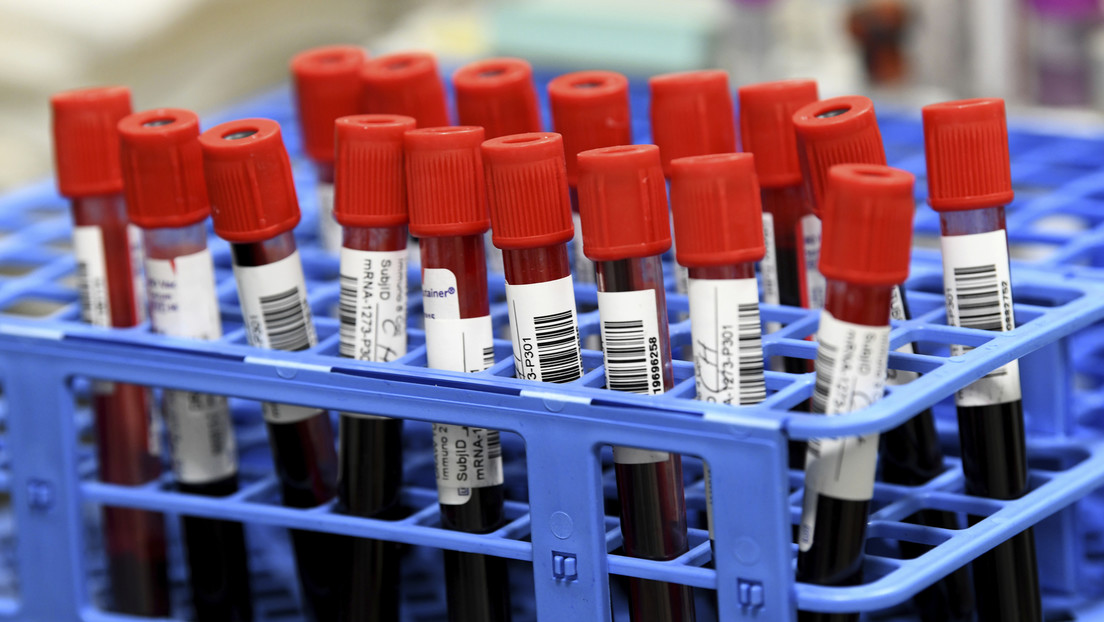
Por otro lado, la vacuna se tolera bien y no existe ningún problema de seguridad hasta la fecha. No obstante, los datos de seguridad continúan acumulándose y el estudio sigue siendo supervisado por una Junta de Supervisión de Seguridad de Datos (DSMB) independiente, designada por el NIH.
Estudio Cove
El estudio de fase 3, conocido como el estudio COVE, inscribió a más de 30.000 participantes en EE UU y se está llevando a cabo en colaboración con el Instituto Nacional de Alergia y Enfermedades Infecciosas (NIAID), que forma parte de los Institutos Nacionales de Salud (NIH), y la Autoridad de Investigación y Desarrollo Biomédico Avanzado (BARDA), que forma parte de la Oficina del Secretario Adjunto de Preparación y Respuesta del Departamento de Salud y Servicios Humanos de los Estados Unidos.
Moderna está trabajando con los Centros para el Control y la Prevención de Enfermedades (CDC) de los Estados Unidos, la Operación Warp Speed y McKesson, un distribuidor de la vacuna COVID-19 contratado por el gobierno de los Estados Unidos, así como con las partes interesadas a nivel mundial para estar preparados para la distribución del mRNA-1273, en caso de que reciba una autorización de uso de emergencia y otras autorizaciones y aprobaciones mundiales similares.

Para finales de 2020, la Compañía espera tener aproximadamente 20 millones de dosis de mRNA-1273 disponibles en los EE.UU. La Compañía sigue en camino de fabricar entre 500 millones y 1.000 millones de dosis a nivel mundial en 2021.
La Compañía enviará los datos del estudio COVE de Fase 3 a una publicación revisada por pares. El criterio de valoración principal del estudio COVE de fase 3 se basa en el análisis de los casos de COVID-19 confirmados y adjudicados a partir de dos semanas después de la segunda dosis de vacuna. La eficacia de la vacuna se ha demostrado en el primer análisis intermedio con un total de 95 casos según el criterio de eficacia preestablecido.
30 casos graves, todos con placebo
El análisis primario de hoy se basó en 196 casos, de los cuales se observaron 185 casos de COVID-19 en el grupo de placebo versus 11 casos observados en el grupo de ARNm-1273, lo que resultó en una estimación puntual de la eficacia de la vacuna del 94,1%.
Un criterio de valoración secundario analizó los casos graves de COVID-19 e incluyó 30 casos graves (como se define en el protocolo del estudio) en este análisis. Los 30 casos ocurrieron en el grupo placebo y ninguno en el grupo vacunado con ARNm-1273. Hubo una muerte relacionada con COVID-19 en el estudio hasta la fecha, que ocurrió en el grupo de placebo.
La eficacia fue constante según la edad, la raza y la etnia, y la demografía de género. Los 196 casos de COVID-19 incluyeron 33 adultos mayores (mayores de 65 años) y 42 participantes que se identificaron como pertenecientes a comunidades diversas (incluidos 29 hispanos o latinos, 6 negros o afroamericanos, 4 asiáticoamericanos y 3 participantes multirraciales).
El perfil de seguridad del estudio de Fase 3 del ARNm-1273 se describió previamente el 16 de noviembre. Se está realizando una revisión continua de los datos de seguridad y la Compañía no ha identificado nuevos problemas de seguridad serios.
Según un análisis anterior, las reacciones adversas solicitadas más comunes incluyeron dolor en el lugar de la inyección, fatiga, mialgia, artralgia, dolor de cabeza y eritema/enrojecimiento en el lugar de la inyección. Las reacciones adversas solicitadas aumentaron en frecuencia y gravedad en el grupo de ARNm-1273 después de la segunda dosis.














